
- English
- Español
- Português
- русский
- Français
- 日本語
- Deutsch
- tiếng Việt
- Italiano
- Nederlands
- ภาษาไทย
- Polski
- 한국어
- Svenska
- magyar
- Malay
- বাংলা ভাষার
- Dansk
- Suomi
- हिन्दी
- Pilipino
- Türkçe
- Gaeilge
- العربية
- Indonesia
- Norsk
- تمل
- český
- ελληνικά
- український
- Javanese
- فارسی
- தமிழ்
- తెలుగు
- नेपाली
- Burmese
- български
- ລາວ
- Latine
- Қазақша
- Euskal
- Azərbaycan
- Slovenský jazyk
- Македонски
- Lietuvos
- Eesti Keel
- Română
- Slovenski
- मराठी
- Srpski језик
กิลเทอริตินิบ ฟูมาเรต
2023-12-02
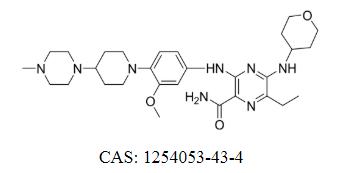
กิลเทอริทินิบ ฟูมาเรต แคส: 1254053-43-4
1. ความเป็นมา
ยาเป้าหมายสำหรับยิลเลตต์ (Gilteritinib) สำหรับผู้ป่วยมะเร็งเม็ดเลือดขาวชนิดเฉียบพลันแบบไมอีลอยด์มีอายุยืนยาวขึ้น ดีขึ้นเมื่อเร็ว ๆ นี้ตีพิมพ์ในวารสารการแพทย์นิวอิงแลนด์เกี่ยวกับผลการทดลองทางคลินิกขนาดใหญ่แสดงให้เห็นว่า: เมื่อเทียบกับเคมีบำบัด การใช้ยาเป้าหมายสำหรับยิลเลตต์ (Gilteritinib ชื่อสินค้าโภคภัณฑ์ การรักษาด้วย Xospata) สามารถปรับปรุงอัตราการรอดชีวิตของผู้ป่วยมะเร็งเม็ดเลือดขาวชนิดเฉียบพลันแบบไมอีลอยด์ (AML) ได้
ผลลัพธ์ของการทดลองครั้งใหม่น่าให้กำลังใจ ผู้ป่วย 371 รายที่ลงทะเบียนในการศึกษานี้คือผู้ป่วย AML ที่มีการกลายพันธุ์เฉพาะของยีน FLT3 ซึ่งเคยได้รับการรักษามาก่อน แต่กลับมาเป็นซ้ำในภายหลังหรือไม่ตอบสนองต่อการรักษา (เกิดซ้ำ/ดื้อต่อการรักษา) พวกเขาได้รับการสุ่มให้ได้รับการรักษาด้วย Gilteritinib หรือเคมีบำบัดมาตรฐาน
ผลการวิจัยพบว่าผู้ป่วยที่รักษาด้วยการใช้ยา Gillett Gilteritinib ไม่เพียงแต่จะมีชีวิตยืนยาวกว่าผู้ป่วยที่ได้รับเคมีบำบัด (ค่ามัธยฐานของเวลารอดชีวิตโดยรวมคือ 9.3 เดือนถึง 5.6 เดือน) และมีแนวโน้มที่จะบรรลุผลการบรรเทาอาการโดยสมบูรณ์ จำนวนเม็ดเลือดขาวกลับสู่ระดับปกติ ทั้งหมดหรือบางส่วน (ผู้ป่วยที่ได้รับการรักษาด้วย Gilteritinib (34%), 15%) ในผู้ป่วยที่ได้รับเคมีบำบัด
2. การนำเสนอ
Gilteritinib Fumarate ซึ่งพัฒนาโดย Astellas ได้รับการอนุมัติจาก Japanese Pharmaceutical Medical Devices And Devices Integrated Agency (PMDA) เมื่อวันที่ 21 กันยายน 2018 ต่อมาได้รับการอนุมัติจากสำนักงานคณะกรรมการอาหารและยาของสหรัฐอเมริกา (FDA) เมื่อวันที่ 28 พฤศจิกายน 2018 และโดยสำนักงานยาแห่งยุโรป (EMA) เมื่อวันที่ 24 ตุลาคม 2562 ภายใต้ชื่อการค้า Xospata® Gilteritinib ได้รับสถานะยาที่รวดเร็วและเป็นยากำพร้าจาก FDA
Gilteritinib Fumarate เป็นตัวยับยั้ง FLT3/AXL และ Xospata® ได้รับการอนุมัติสำหรับการรักษามะเร็งเม็ดเลือดขาวชนิดเฉียบพลันแบบไมอีลอยด์ที่เกิดซ้ำหรือดื้อต่อการรักษา โดยมีการกลายพันธุ์ของ FLT3 เป็นบวก
Xospata® เป็นยาเม็ดชนิดรับประทานที่มี Gilteritinib 40 มก. ปริมาณที่แนะนำคือ 120 มก. วันละครั้ง เพิ่มหรือลดขนาดยาตามอาการของผู้ป่วย แต่ไม่ควรเกิน 200 มก. ต่อวัน
3. จุดเป้าหมาย
แอ๊กซ์แอล; FLT3
4. กลไกการออกฤทธิ์
สารยับยั้งตัวรับ AXL; สารยับยั้ง FLT3
5. ข้อบ่งชี้
มะเร็งเม็ดเลือดขาวชนิดเฉียบพลันแบบไมอีลอยด์
6. ขั้นตอนการพัฒนา
อนุมัติให้ทำการตลาดเมื่อ 21 กันยายน 2561
7. บริษัทวิจัยและพัฒนา
แอสเทลลัส
8. เส้นทางการสังเคราะห์
8.1. เส้นทางเดิม
8.2. เส้นทางของเรา (ปรับให้เหมาะสม) - เสถียรภาพที่ดีขึ้นและให้ผลตอบแทนที่สูงขึ้น
8.3. ดอกกุหลาบ ของ KSM [CAS 2043020-03-5]
8.4. กระบวนการผลิตโดยย่อ [CAS 2043020-03-5]
ขั้นตอนที่ 1:
ไปยังสารแขวนลอยของ NaOH ถูกเติมเอทิล 3-ออกโซเพนทาโนเอตในส่วนเดียว, และจากนั้นของผสมปฏิกิริยาถูกกวนที่อุณหภูมิห้อง เติมสารละลาย NaNO2 ในน้ำ จากนั้นเติม H2SO4 แบบหยดลงไป สารละลายของ NaOH ถูกเติมแบบหยด และของผสมที่เป็นผลลัพธ์ถูกสกัดด้วย MTBE ชั้นอินทรีย์ที่รวมกันถูกล้างด้วยน้ำเกลือ, ทำให้แห้งบน Na2SO4, กรองและทำให้เข้มข้นเพื่อให้ผลิตภัณฑ์ (E)-2-ออกโซบิวแทนอล ออกไซม
ขั้นตอนที่ 2:
สารแขวนลอยของ (E)-2-oxobutnal oxime และ Aminomalononitrile p-Toluenesulfonic Acid ใน IPA ) ถูกกวนที่อุณหภูมิห้องภายใต้อาร์กอน หลังจากตรวจสอบโดย TLC แล้ว ของผสมของปฏิกิริยาถูกกรอง, เค้กถูกล้างด้วย IPA และน้ำ และทำให้แห้งเพื่อให้ได้ 2-อะมิโน-3-ไซยาโน-5-เอทิลไพราซีน 1-ออกไซด์
ขั้นตอนที่ 3:
ไปยังสารแขวนตะกอนของ 2-อะมิโน-3-ไซยาโน-5-เอทิลไพราซีน 1-ออกไซด์ในแอนไฮดรัส DMF ถูกเติม POCl3 ที่ 0oซ ของผสมที่เป็นผลลัพธ์ถูกกวนผสมที่ 80oC หลังจากตรวจสอบโดย TLC แล้ว ของผสมปฏิกิริยาถูกเติมลงในน้ำแข็ง/น้ำอย่างช้าๆ และสกัดด้วย MTBE ชั้นอินทรีย์ที่รวมกันถูกล้างด้วยน้ำเกลือ, ทำให้ Na2SO4 แห้ง, กรองและทำให้เข้มข้นเพื่อให้ได้ 3-อะมิโน-5-คลอโร-6-เอทิลไพราซีน-2-คาร์โบไนไทรล์
ขั้นตอนที่ 4:
สารแขวนลอยของ t-BuONO และ CuBr2 ใน DMF ถูกเติมด้วยสารละลายของ 3-อะมิโน-5-คลอโร-6-เอทิลไพราซีน-2-คาร์โบไนไตรล์ใน DMF แบบหยด หลังจากตรวจสอบโดย TLC แล้ว ของผสมปฏิกิริยาถูกทำให้เย็นลงจนถึงอุณหภูมิห้อง และจากนั้นเทลงในน้ำแข็ง/น้ำ สกัดด้วย MTBE ชั้นอินทรีย์ที่รวมกันถูกล้างด้วยน้ำเกลือ, ทำให้ Na2SO4 แห้ง, กรองและทำให้เข้มข้นเพื่อให้สารดิบซึ่งถูกทำให้บริสุทธิ์โดยโครมาโทกราฟีเพื่อให้ได้ 3-โบรโม-5-คลอโร-6-เอทิลไพราซีน-2-คาร์โบไนไทรล์
9. รายชื่อตัวกลางที่เราสามารถจัดหาได้
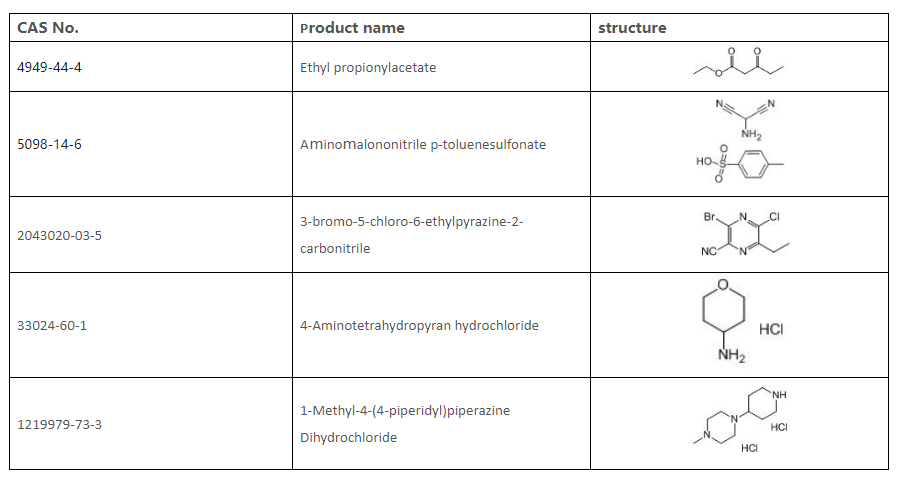
Sandoo Pharmaceutica คือผู้ผลิตตัวกลางทางเภสัชกรรมระดับมืออาชีพ เราจัดหา Gilteritinib Fumarate Cas: 1254053-43-4 คุณภาพดี ยินดีต้อนรับและเราหวังว่าจะมีคำถามของคุณ!




